醫療器械研發工程師入門知識,,機械設計基礎知識,醫療器械開發流程大概分為八個步驟(產品需求、系統需求、研發設計、測試驗證、型式檢測、設計凍結、臨床試驗、注冊拿證、機電部件開發流程)。這八個步驟完成后,一款新的醫療器械就可以獲批上市了。首先是產品需求確定,這個是由產品經理來進行定義,主要通過市場的調研,臨床應用場景,醫生拜訪,產品經理需要對產品的整個工作流行定義和澄清。產品經理的需求會傳遞給系統工程部,由系統工程師承接,然后降產品的需求轉化為工程技術指標。這個過程中,系統工程師需要完成系統功能架構和組成部件的劃分,除此之外,還需要輸出法規和標準,風險安全性、可用性、可服務性。和可制造性等相關的需求來對系統進行約束,確保系統可以滿足醫療器械的要求。
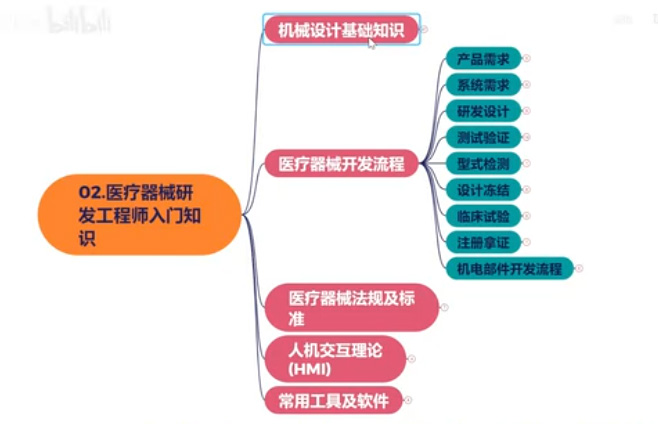
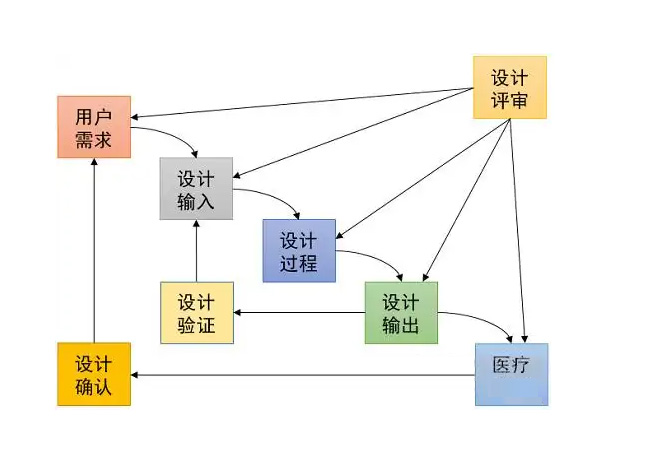
系統需求由器械研發工程師承接,器械研發工程師需要將系統需求轉化為不見設計規范。并對系統指標進行分解。細化為不見設計的指標。并且定義這些指標的測試方法。然后進行部件結構的設計、打樣驗證和優化迭代工作。測試的目的是為了驗證部件系統的設計是不是滿足產品的要求。分為了不見測試、集成測試、系統測試、法規測試、風險測試、可用性測試、內部動物試驗。都是為了不見跟系統的確認。確保設計要符合要求。這些測試項目都通過后就可以進行國家藥監局的檢測了。型式檢測通過,需求文檔、設計規范、物料驗證、BOM、圖紙、測試文檔及報告、工藝SOP等凍結受控。將研發狀態轉換成為可以量產狀態。小批量試產,為臨床試驗做好準備。生產的樣機需要完成臨床試驗的驗證。動物臨床試驗,臨床數據分析等。動物試驗是為臨床試驗做準備。通過臨床試驗、醫生使用器械在病患身上做手術。確認系統功能滿足臨床使用要求。試驗期間的臨床數據和醫生的反饋。作為下一代產品研發需求的輸入。進行產品的迭代。臨床試驗通過后,提交臨床數據和,型式檢測報告,在國家藥監局提交,注冊申請,拿證獲批后即可上市。醫療器械法規及標準,人機交互理論,常用工具跟軟件。
聯系人:13922709440 余先生
銷售熱線:0724-4016818
售后服務:19171569097
服務熱線:400-800-8232
郵 箱:xianhao266@163.com
公 司:湖北省顯浩裝備科技有限公司
地 址:湖北省鐘祥市南湖新區協企聯盟產業園C6棟